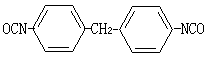胺的释义:氨分子中的一个或多个氢原子被烃基取代后的产物,称为胺。根据胺分子中氢原子被取代的数目,可将胺分成伯胺、仲胺、叔胺。例如:CH3CH2NH2(伯胺) (CH3CH2)2NH(仲胺) (CH3CH2)3N(叔胺) 氨分子中的氢被烃基取代而生成的化合物。 胺可以是看作氨分子中的H被烃基取代的衍生物。胺类广泛存在于生物界,具有极重要的生理活性和生物活性,如蛋白质、核酸、许多激素、抗生素和生物碱等都是胺的复杂衍生物,临床上使用的大多数药物也是胺或者胺的衍生物,因此掌握胺的性质和合成方法是研究这些复杂天然产物及更好地维护人类健康的基础。 基本解释 胺(àn) 氨NH3分子中部分或全部氢原子被烃基取代后而成的有机化合物,胺类大都具有碱性,能与酸结合而成盐,是制作合成染料、药物等的原料。 详细解释 胺 【名】 氨分子里的氢被烃基或其他非酸性有机基取代后衍生出的一类有机化合物〖amine〗 胺 (è )【动】 肉类腐烂变臭〖(ofmeat)putrefy〗。 《广韵》:“胺,肉败臭。”
-
胺的分类
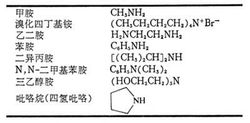
按照氢被取代的数目,依次分为一级胺(伯胺)RNH2、二级胺(仲胺)R2NH、 三级胺(叔胺)R3N、四级铵盐(季铵盐)R4N+X-,例如甲胺CH3NH2、苯胺C6H5NH2、乙二胺H2NCH2CH2NH2、二异丙胺[(CH3)2CH]2NH、三乙醇胺(HOCH2CH2)3N、溴化四丁基铵(CH3CH2CH2CH2)4N+Br-。根据胺分子中与氮原子相连的羟基种类的不同,胺可以分为脂肪胺和芳香胺。根据胺分子中与氮原子相连的羟基的数目,可以分为一级胺(伯胺,primary amine)、二级胺(仲胺,secondary amine)和三级胺(叔胺,tertiary amine)。如果胺分子中含有两个或两个以上的氨基(—NH2),则根据氨基数目的多少,可以分为二元胺、三元胺。
胺的物化性质
在常温下,低级脂肪胺是气体,丙胺以上是液体,高级脂肪胺是固体。低级胺有令人不愉快的,或是很难闻的气味。例如三甲胺有鱼腥味,丁二胺(腐胺)和戊二胺(尸胺)有动物尸体腐烂后的恶臭味。高级胺不易挥发,气味很小。芳胺为高沸点液体或低熔点固体,气味虽比脂肪胺小,但毒性比较大,无论是吸入他们的蒸气或皮肤与之接触都会引起中毒。有些芳胺,如β-萘胺,联苯胺还有致癌作用。由于胺分子中的氮原子能与水形成氢键,所以低级脂肪胺在水中的溶解度都比较大。伯胺和仲胺能形成分子间的氢键,但由于氮原子的电负性小于氧原子,所以胺的氢键缔合能力比较弱,其沸点比相对分子质量相近的醇低。R-NH 2+HCl≒R-NH 3 +Cl - -
合成
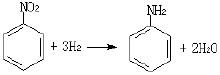
卤化物氨解(Ammonolysis of halides)氨或胺氮上有孤对电子,作为亲核试剂与卤代烷发生亲核反应,按SN2机理进行。许多有机卤化物以氨水溶液或氨溶液处理则变成胺类:X为卤素RX + NH3 → RNH3 + X-RNH3+X- → RNH2 + H2O + X-用醇制备胺的主要合成方法是氨的烷基化。工业上使用醇与氨合成有机胺:ROH + NH3 → RNH2 + H2O这些反应需要使用催化剂、特制仪器及额外纯化,因为得到的是一、二、三级胺的混合物,需要提高反应的选择性。
- 胺的制法
-
胺的应用
胺的用途很广。最早发展起来的染料工业就是以苯胺为基础的。有些胺是维持生命活动所必需 的,但也有些对生命十分有害,不少胺类化合物有致癌作用,尤其是芳香胺,如萘胺、联苯胺等。
- 命名
-
胺的结构
实验证明,胺和氨分子具有棱形锥形结构,氮原子为sp3杂化,键角约为109度。在胺分子中,三个sp3杂化轨道分别于氢原子的s轨道或碳原子的杂化轨道重叠形成三个6键,剩下一对孤对电子占据第四个sp3轨道,位于棱椎体的顶端。制法胺在自然界中分布很广,其中大多数是由氨基酸脱羧生成的,例如: