G蛋白是指能与鸟嘌呤核苷酸结合,具有GTP水解酶活性的一类信号转导蛋白。G蛋白参与的信号转导途径在动植物体中是一种非常保守的跨膜信号转导机制。当细胞转导胞外信号时,首先由不同类型的G蛋白偶联受体(GPCRs)接受细胞外各种配基(胞外第一信使)。然后受体被活化,进一步激活质膜内侧的异三聚体G蛋白,后者再去激活其下游的各种效应器,产生细胞内的第二信使。从而将信号逐级传递下去,调节生物体的生长发育过程。 在细胞内信号传导途径中起着重要作用的GTP结合蛋白,由α,β,γ三个不同亚基组成。激素与激素受体结合诱导GTP跟G蛋白结合的GDP进行交换结果激活位于信号传导途径中下游的腺苷酸环化酶。G蛋白将细胞外的第一信使肾上腺素等激素和细胞内的腺苷酸环化酶催化的腺苷酸环化生成的第二信使cAMP联系起来。G蛋白具有内源GTP酶活性。
-
介绍
G蛋白是细胞内信号传导途径中起着重要作用的GTP结合蛋白,由α,β,γ三个不同亚基组成。激素与激素受体结合诱导GTP跟G蛋白结合的GDP进行交换结果激活位于信号传导途径中下游的腺苷酸环化酶。G蛋白将细胞外的第一信使肾上腺素等激素和细胞内的腺苷酸环化酶催化的腺苷酸环化生成的第二信使cAMP联系起来。G蛋白具有内源GTP酶活性。
-
读取信息
细胞间通过传递信号分子相互交流。有些信号分子可以通过血液在体内进行远距离传输;另一些在邻近细胞间传递。人体中存在成千上万种信号分子,常见的如控制兴奋水平的肾上腺素,传递血糖水平的高血糖素,标志组织损伤的组胺和在神经系统中传递信息的多巴胺。
-
蛋白分类
G蛋白的种类已多达40余种,大多数存在于细胞膜上,由α、β、γ三个不同亚单位构成,总分子量为100kDa左右。其中β亚单位在多数G蛋白中都非常类似,分子量36kDa左右。γ亚单位分子量在8-11kDa之间,除Gt外,大多数G蛋白的γ亚单位都是相同的。βγ两个亚单位的不同可以将G蛋白分为Gs、Gi、Go、Gq、G?及Gt等六类。这些不同类型的G蛋白在信号传递过程各种发挥不同的作用。除此之外,在细胞内还存在另一类G蛋白,这类G蛋白具有鸟核苷酸的结合位点,有GTP酶活性,其功能也受鸟核苷酸调节,但与跨膜信息传递似乎没有直接相关。在结构上不同于前述的G蛋白,分子量较小,在20-30kDa之间,不是以α、β、γ三聚体方式存在,而是单体分子,因此被称为 小G蛋白(small G proteins)。如ras表达产物为一种小G蛋白。小G蛋白同ras蛋白具有同源性,同属于ras超家族(ras superfamily)。哺乳动物G蛋白中属ras超家族约有50多个成员,根据它们序列同源性相近程度又可以分为Ras、Rho和Rab三个主要的亚家族。
- 蛋白调控
-
细胞膜
附着于G蛋白链的一些小分子类脂(图右上部),嵌入细胞膜,使G蛋白结合于细胞内膜表面,与受体接近。蛋白质结晶时这些类脂被除去,因此晶体结构中不显示。
-
攻击
G蛋白系统是许多信号传递途径的中心环节,因此也就成了众多药物和毒素攻击的靶位点。市面上的很多药物,如Claritin和Prozac,以及大量滥用的毒品:可卡因,海洛因,大麻等,通过与G蛋白偶联进入细胞发挥其药性。霍乱菌产生一种毒素,与G蛋白处在关键位置的核苷结合,使G蛋白处于持续活化状态,破坏肠细胞液体平衡的正常调控。感染者因身体丧失水,钠和氯化物而脱水。信号接力G蛋白位于细胞膜内表面。当受体同激素或神经递质结合后,信息传递过程起始。如结合肾上腺素后,受体首先改变形状,与细胞内非活性状态的G蛋白结合。这种结合使G蛋白放弃GDP,接受GTP。 GTP使一个小的环状结构变形,G蛋白分解成两部分——其中携带GTP的α亚基沿膜移动直至遇到腺苷酸环化酶,小的环状结构与腺苷酸环化酶结合并将其激活。活化后的腺苷酸环化酶产生大量cAMP(环腺苷酸)分散到细胞内——传达信息。最终,GTP水解成GDP,G蛋白重新组装,恢复非活性状态。这种信号传递途径的最大优点是使信号加强。与信号传递链中的酶(如腺苷酸环化酶)结合后,细胞外微弱的信号在胞内被转换成强信号。在前面的例子中,仅一个肾上腺素分子就可以激生大量的cAMP.结构探索GTP是G蛋白活性状态的开关。在活性状态,GTP的最后一个磷酸基团与G蛋白表面的环状结构相连,使环处于紧密状态。当GTP水解成GDP时,这个磷酸基被移去,GDP变短不能与此环相连,导致环结构松散,转变为非活性三聚体,如图左蛋白质编码1gg2。
-
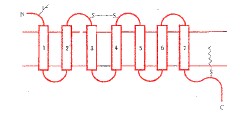
传递
细胞表面的受体通过与其相应配体作用后,可经不同种类的G蛋白偶联,分别发挥不同的生物学效应。与G蛋白偶联的多种 受体具有共同的结构功能特点:分子量40-50kDa左右,由350-500氨基酸组组成,形成7个由疏水氨基酸组成的α螺旋区段,反复7次穿越细胞膜的脂质双层。肽链的N末端在胞膜外,C末端在细胞内。N末端上常有许多糖基修饰。从功能上看,受体的识别区域并不象一般想象的那样在胞膜的外部,实际上是由7个跨膜区段间通过特定氨基酸残基之间的相互作用形成复杂的空间构象。配体结合于识别区域之后,即导致整个受体构象的变化。受体肽链的C末端和连接第5和第6个跨膜区段的第三个胞内环是G蛋白结合部位。目前研究发现,趋化因子受体家族(chemokine receptor family)以及一些神经递质受体都属于G蛋白偶联的7次跨膜受体的超家族。例如IL-8RA胞膜外N端Asp11、Llu275、Arg280以及可形成二硫键的Cys30和Cys277在与配体结合中起重要作用;紧接第三个空膜区第二个胞浆环中DRY序列对于与G蛋白的结合是必要的。(3)Gt:可以激活cGMP磷酸二酯酶,同视觉有关。(4)Go:可以产生百日咳杆菌毒素导致的一系列效应。
- G-蛋白概念